Прицельная биопсия:
Эрозии:
· отмечается дефект многослойного плоского эпителия инфильтрированная лейкоцитами. В дне эрозии наблюдается разрастание грануляционной ткани и инфильтрация из полиморфноядерных лейкоцитов, гистиоцитов, а также отмечается полнокровие сосудов и набухание эндотелия.
Эктопии:
· различают железистые, папиллярные и незрелая плоскоклеточная метаплазия. Железистая характеризуется наличием железистых структур в подэпителиальной ткани, высокий цилиндрический эпителий выстилает ветвящиеся железистые ходы – эрозионные железы, вокруг которых отмечается воспалительная реакция. Папиллярная – характеризуется разрастанием стромы с формированием сосочков различной величины, покрытых цилидрическим эпителием.
Эктропион:
· метаплазия цилиндрического эпителия цервикального канала многослойным плоским, возможно разрастание соединительной ткани;
· выскабливание цервикального канала с последующим исследованием соскоба – отсутствие атипичных клеток.
- Эрозия, эктопия и эктропион шейки матки
- Клиническая картина
- Cимптомы, течение
- Диагностика
- Лабораторная диагностика
- Доброкачественные и предраковые заболевания шейки матки с позиции профилактики рака
- Современные аспекты патогенеза доброкачественных и предраковых заболеваний шейки матки (обзор литературы)
- Современная диагностика предраковых состояний шейки матки.
- Причины появления рака шейки матки и факторы риска
- Стадии рака шейки матки и прогнозы выживаемости
- Значение скрининга в диагностике предрака и рака шейки матки
Эрозия, эктопия и эктропион шейки матки

Классификация эрозии (истинной эрозии):
· воспалительная;
· травматическая;
· трофическая (при наличии опущения и выпадения шейки матки).
По этиопатогенезу:
· врождённая (влияние высокого уровня гормонов материнского организма);
· приобретённая (в период пубертата отмечается быстрый рост мышечных структур шейки матки с отставанием пролиферативного процесса в многослойном плоском эпителии).
По клиническому течению:
· неосложнённая форма;
· осложнённая форма (сочетание с цервицитом, вагинитом);
По гистологическому строению:
· железистая (фолликулярная) – множество железистых ходов;
· папиллярная (сосочковая) – разрастание стромы;
· эпидермизирующая (заживающая) – участки цилиндрического эпителия замещаются многослойным плоским в результате метаплазии резервных клеток или «наползания» клеток плоского эпителия с периферии на зону эктопии.
Клиническая картина
Cимптомы, течение
Жалобы и анамнез (характер возникновения и проявления болевого синдрома)[2]:
Жалобы:
· слизистые выделения из половых путей;
· гноевидные выделения из половых путей;
· межменструальные кровянистые выделения из половых путей;
· контактные кровянистые выделения из половых путей.
Анамнез:
· наличие онкозаболеваний у близких родственников;
· особенности менструальной детородной функции (количество родов, абортов, характер контрацепции);
· перенесенные гинекологические заболевания (срок и длительность выявления патологии шейки матки).
При гинекологическом осмотре:
Эрозия: дефект слизистой наружного зева ярко красного цвета, неправильной формы, относительно четкими границами, легко травмируется, кровоточит.
Эктопия: дефект слизистой наружного зева с неправильными очертаниями от ярко-красного до бледно-розового цвета. Возможна значительная гиперемия, наботовые железы, отек.
Эктропион: характеризуется выворотом слизистой оболочки цервикального канала. Шейки матки может быть гипертрофирована с наличием рубцовой деформации.
Диагностика
Перечень основных и дополнительных диагностических мероприятий:
Основные (обязательные) диагностические обследования, проводимые на амбулаторном уровне [2]:
· сбор жалоб и анамнеза;
· физикальное обследование – общий гинекологический осмотр;
· мазок на степень чистоты влагалища;
· цитологическое исследование мазков с шейки матки (ПАП – тест);
· кольпоскопия.
Дополнительные диагностические обследования, проводимые на амбулаторном уровне [2]:
· ОАК с определением времени свертываемости крови;
· микрореакция;
· ВИЧ (при подготовке к хирургическому лечению);
· жидкостное цитологическое исследование соскоба шейки матки и цервикального канала;
· ПЦР на хламидии (ВПЧ 16, ВПЧ 18, ВПГ 2 – для определения онкогенного риска вируса папилломы человека) (УД – IIIС);
· прицельная биопсия (для верификации диагноза при подозрении на интраэпителиальную неоплазию, рекомендуется производить забор ткани с патологического участка под контролем кольпоскопии) (УД – IA);
· выскабливание цервикального канала с последующим исследованием соскоба (необходим в случаях, когда не визуализируется стык цилиндрического и многослойного плоского эпителия, при результате ПАП – теста AGC, и у женщин старше 45 лет) (УД – IIВ).
Расширенная кольпоскопия/видеокольпоскопия [4,5,6,7]:
Эрозия:
· дефект эпителия с обнаженной подэпителиальной стромой с четкими краями, в котором обнаруживаются признаки воспалительной реакции: расширение каппиляров, нарушение микроциркуляции, отечность. После применения раствора уксусной кислоты дно эрозии бледнеет, после раствора Люголя – дно не окрашивается.
Эктопия:
· отмечается смещение цилиндрического эпителия на экзоцервикс с зоной трансформации (зона превращения), которая характеризуется наличием метапластического эпителия различной степени зрелости, открытых и закрытых желез, островков цилиндрического эпителия с нечеткими контурами, иногда с сосудистой сети.
Эктропион:
· обнаруживается выворот и обнажение слизистой цервикального канала, при котором может нарушаться граница между многослойным плоским и цилиндрическим эпителием шейки матки.
Прицельная биопсия:
Эрозии:
· отмечается дефект многослойного плоского эпителия инфильтрированная лейкоцитами. В дне эрозии наблюдается разрастание грануляционной ткани и инфильтрация из полиморфноядерных лейкоцитов, гистиоцитов, а также отмечается полнокровие сосудов и набухание эндотелия.
Эктопии:
· различают железистые, папиллярные и незрелая плоскоклеточная метаплазия. Железистая характеризуется наличием железистых структур в подэпителиальной ткани, высокий цилиндрический эпителий выстилает ветвящиеся железистые ходы – эрозионные железы, вокруг которых отмечается воспалительная реакция. Папиллярная – характеризуется разрастанием стромы с формированием сосочков различной величины, покрытых цилидрическим эпителием.
Эктропион:
· метаплазия цилиндрического эпителия цервикального канала многослойным плоским, возможно разрастание соединительной ткани;
· выскабливание цервикального канала с последующим исследованием соскоба – отсутствие атипичных клеток.
Показания для консультации узких специалистов:
· консультация онколога при выявлении тяжелой цервикальной интраэпителиальной неоплазии, атипических железистых клеток и при подозрении на рак шейки матки.
Лабораторная диагностика
Основные:
· мазок на степень чистоты влагалища (наличие воспалительного процесса во влагалище);
· цитологическое исследование мазков с шейки матки/ПАП тест (отсутствие атипичных клеток и интраэпителиальной неоплазии) смотрите приложение 1. Интерпретация результатов цитологического исследования, согласно терминологической системе Бетезда [3,4,5] смотрите приложение 2.
· жидкостное цитологическое исследование соскоба шейки матки и цервикального канала – отсутствие интраэпителиальных неоплазий со слизистой цервикального канала и влагалищной части шейки матки;
· ПЦР-диагностика на хламидии, ВПЧ 16, ВПЧ 18, ВПГ 2 (определение наличия или отсутствие вируса папилломы человека);
· бактериологическое исследование для идентификации микрофлоры (определяет наличие инфекционного агента и его чувствительность к противомикробным средствам).
Хочу сказать большое спасибо и благодарность массажисту Тимофею. Прошла курса массажа у него и очень довольно его работой.Все мой проблемы со спиной были устранены ,я снова стала жить.Тимофей очень позитивный человек, хорошая энергетика , профессионал своего дела.
Доброкачественные и предраковые заболевания шейки матки с позиции профилактики рака
В России созданы собственные клинические рекомендации по диагностике и ведению пациентов с патологией шейки матки. Врачи медицинского центра “Гармония” работают в соответствии со стандартами.
Уважаемые коллеги, предлагаем и вам ознакомиться с документом:
Поздравляю с днем медицинского работника всех сотрудников гинекологического отделения ул.Советская 42. Спасибо вам за ваш труд! Здоровья и исполнения желаний! Низкий поклон и благодарность врачам: Абакумовой Е.И., Плотко Е.Э. , Яковлеву С.Н., Хлебниковой И.В., Федотовой Е.А. !
Хочу сказать большое спасибо и благодарность массажисту Тимофею. Прошла курса массажа у него и очень довольно его работой.Все мой проблемы со спиной были устранены ,я снова стала жить.Тимофей очень позитивный человек, хорошая энергетика , профессионал своего дела.
Очень рады, что нашли в Вашем центре совершенно замечательного педиатра Сигал Людмилу Феликсовну. Ребенок маленький – 6 месяцев. Поэтому масса вопросов, сомнений и тревог, которые искренне помогает разрешить Ваш очаровательный доктор. Очень благодарны за чуткое, терпимое и доброжелательное отношение к деткам и их родителям. Крайне приятно приходить на прием к врачу, который излучает тепло и доброту. Берегите, пожалуйста, такие ценные для Вас и, конечно же, для нас кадры. С искренним уважением и благодарностью Ган Е.Ю.
8. Киселев В.И., Ашрафян Л.А., Бударина С.О., Киселев О.И, Пальцев М.А., Кулаков В.И., Прилепская В.Н. Этиологическая роль вируса папилломы человека в развитии рака шейки матки: генетические и патогенетические механизмы, возможности терапии профилактики. М.: «Медиа Медика». Гинекология, 2004; Т. 6, №4. С. 174-180.
Современные аспекты патогенеза доброкачественных и предраковых заболеваний шейки матки (обзор литературы)
Резюме
Патологические процессы шейки матки относятся к актуальным вопросам современной гинекологии в связи с тем, что они часто трансформируются в злокачественные заболевания и нередко отмечаются в репродуктивном возрасте. Доброкачественные заболевания не являются причиной развития опухоли, однако часто предшествуют предраковым процессам. Одним из важных событий необходимых для развития опухолевого роста играют эпигенетические нарушения, к которым относят метилирование генов-супрессоров опухолевого роста. Комплексная оценка клинических особенностей доброкачественных и предраковых процессов шейки матки в совокупности с результатами исследования метилирования генов позволит разработать принципы прогнозирования риска по возникновению онкопатологии шейки матки.
Ключевые слова
шейка матки, доброкачественные и предраковые процессы, вирус папилломы человека, метилирование генов.
1. Аполихина И.А., Е.Д.Денисова, Г.Н.Ворожцов, С.Г.Кузьмин. Лечебные и профилактические аспекты папилломавирусной инфекции гениталий. Эффективная фармакотерапия в акушерстве и гинекологии. М.:«Медиа Медика». Гинекология, 2009; №1. С. 26-30.
2. Ашрафян Л.А., Киселев В.И. Опухоли репродуктивных органов (этиология и патогенез). М.: Димитрейд График Групп, 2008. С.216.
3. Залетаев Д.В., Немцова М.В., Бочков Н.П. Метилирование ДНК как этиологический фактор канцерогенеза. Вестник РАМН. М., 2002. №4. С. 6-11.
4. Залетаев Д.В., Немцова М.В., Стрельников В. 2004 Диагностика эпигенетической патологии при наследственных и онкологических заболеваниях. Молекулярная биология. 38, 213-223.
5. Кекеева Т.В., Жевлова А.И., Подистов Ю.И., Соловьева Ю.В., Залетаев Д.В., Немцова М.В. Аномальное метилирование генов-супрессоров опухолевого роста как потенциальный маркер предраковых состояний шейки матки. Клиническая лабораторная диагностика. М., «Медицина». 2006. №3. С.46-49.
6. Киселев Ф.Л., Мазуренко Н.Н., Волгарева Г.Н., Киселева Н.П. Взаимодействие вирусных и клеточных генов в опухолях шейки матки. Молекулярная биология. М., «Наука». 2004. Т. 38. №2. С. 224-232.
7. Киселев В.И., Аполихина И.А., Муйжнек Е.Л. и др. Патогенетические подходы к лечению ВПЧ-ассоциированных заболеваний шейки матки. Патология шейки матки и генитальные инфекции под ред. В.Н.Прилепской. М., «МЕДпресс-информ», 2008. С.87-94.
8. Киселев В.И., Ашрафян Л.А., Бударина С.О., Киселев О.И, Пальцев М.А., Кулаков В.И., Прилепская В.Н. Этиологическая роль вируса папилломы человека в развитии рака шейки матки: генетические и патогенетические механизмы, возможности терапии профилактики. М.: «Медиа Медика». Гинекология, 2004; Т. 6, №4. С. 174-180.
9. Киселев В.И. Молекулярные механизмы патогенеза гиперпластических и диспластических заболеваний репродуктивной системы и пути их фармакологической коррекции. Патология шейки матки и генитальные инфекции под ред. В.Н.Прилепской. М., «МЕДпресс-информ», 2008. С. 53-60.
10. Лихтенштейн А.В., Киселева Н.П. Биохимия. М. , 2001. 66 (3). С. 657-69.
11. Мазуренко Н.Н., Блиев Ю., Биджиева Б. Молекулярная биология. М.,«Наука». 2006. Т.40. С. 436-47.
12. Молочков В.А., Киселев В.И., Рудых И.В., Щербо С.Н. Папилломавирусная инфекция – клиника, диагностика, лечение. М.: Студия «Мирада Вива», 2005. С. 5-9.
13. Прилепская В.Н. Патология шейки матки и генитальные инфекции. Под ред. В.Н. Прилепской. М., «МЕДпресс-информ», 2008. 383 с.
14. Прилепская В.Н., Голубенко А.Е. Эпидемиология, этиология и факторы риска заболеваний рака шейки матки. Поликлиническая гинекология под ред. проф. В.Н. Прилепской. М.,2005. С.9-20.
15. Подистов Ю.И., Лактионов К.П., Петровичев Н.И., Брюзгин В.В. Эпителиальные дисплазии шейки матки (диагностика и лечение). М.: ГЭОТАР-Медиа, 2006.
16. Роговская С.И., Прилепская В.Н., Кондриков Н.И., Ежова Л.С. Клинико- морфологические особенности папилломавирусной инфекции гениталий у женщин. М.: «Медиа Медика». Гинекология, 2004; Т.6, № 2: 57-59.
17. Фролова И. И., Местергази Г.М., Радзинский В.Е., Шелястина Н.И., Бабиченко И.И. Иммуногистохимические исследования дискератоза и неопластических изменений экзоцервикса при гинекологической патологии. Архив патологии. М., «Медицина». 2002. №6. Т.64. С.23-27.
18. Ходырев Д.С. Изменение метилирования промоторных областей семи генов хромосомы 3 человека в эпителиальных опухолях. Автореф. дис. на соиск. уч. ст. канд. биол. наук. М.,2009.
19. Chan A.O., Kim S.G., Bedeir A. CpG Island methylation in carcinoid and pancreatic endocrine tumors. Oncogen 2003. Feb13; 22(6):924-934.
20. Cheung T.H ., Lo K.W., Yim S.F. Epigenetic and genetic alternation of PTEN in cervical neoplasm. Gynecol Oncol, 2004. Jun; 93(3):621-627.
21. Choy K.W., Chi Pui Pang, Ka Fai To, Christofer B.O. Yu, Joan S.K. Ng, Dennis S.G.Lam et al. Impaired Expression and Promotor hypermethylation of O6-methylguanine-DNA methyltransferase in Retinoblastoma tissues. Investigative Ophthalmology and Visual Science. 2002: 43: 1344-1349.
22. Duffy M., Napieralski R., Martens J., Span P., Spyratos F., Sweep F., Brunner N., Foekens J., Schmitt M. Methylated genes as new cancer biomarkers. European Journal of Cancer. 2008. Vol. 45. Issue 3. P. 335-346.
23. Esteller M., Corn P.G., Baylin S.B., Herman J.G. A Gene hypermethylation profile of human cancer. Cancer Research 2001. Vol.61. P.3225-3229.
24. Fenton S.L., Dallol A., Agathanggelou A., Hesson L., Ahmed-Choudhury J., Baksh S., Sardet C., Dammann R., Minna J.D., Downward J., Maher E.R., Latif F. Identification of the E1A-regulated transcription factor p120 E4F as an interacting partner of the RASSF1A candidate tumor suppressor gene. Cancer Res. 2004 Jan 1:(64):102-7.
25. Ferlay J., Bray F., Pisani P., Parkin D.M. Cancer incidence, mortality and prevalence worldwide. GLOBOCAN 2002: Version 1.0/ IARC Cancer Base NS №5. Lyon: IARCPress (www-dep.iarc.fr).
26. Fiedler M., Muller-Holzner E., Viertler H.P. et al. (2004) High level HPV-16 E7 oncoprotein expression correlates with reduced pRb-levels in cervical biopsies. FASEB J, 18(10), 1120-1122.
27. Focchi G.R., Silva I.D., Nogueira-de-Souza N.C., Dombo C., Oshima C.T., Stavale J.N. Immunohistochemical expression of p16 (INK4A) in normal uterine cervix, nonneoplastic epithelial lesions, and low-grade squamous intraepithelial lesions. J Low Genit Tract Dis. 2007 Apr. 11(2):98-104.
28. Gonkong C.S., Balcer B.L., Troxe M.L., Patterson K., Longacre T.P. Immunohistochemical superior HPV on the site of hybridization for the detection of high risk HPV in atypical squamous cell metaplasia. Am J Surg Pathol. 2007. Jan; 31 (1): 33-43.
29. House M., Guo M., Iacobuzio-Donahue C., Herman J. Molecular progression of promoter of promoter methylation in intraductal papillary mucinous neoplasms of the pancreas. Carcinogenesis. 2003. Feb 24(2): 193-198.
30. Hitchins M.P., Wong J.J., Suthers G., Suter C.M., Martin D.I., Hawkins N.J., Ward R.L. Inheritance of a cancer-associated MLH1 germ-line epimutation. N Engl J Med. 2007 Feb 15; 356(7):697-705.
31. Jeon J.H., Shin D.M., Cho S.Y., Song K.Y., Parc N.H., Kang H.S., Kim Y.D., Kim I.G. Immunocytochemical detection of HPV 16 E7 in cervical smear. Exp Mol Med. 2007. Oct 31; 39 (5):621-8.
32. Kausar M. Neyaz, R. Suresh Kumar, Showket Hussain et al. Effect of aberrant promoter methylation of FHIT and RASSF1A genes on susceptibility to cervical cancer in a North Indian population. 2008. Vol. 13. №6. Pages 597- 606.
33. Kim M., Kang H.G., Lee S.Y., Lee H.C., Choi Y.Y., Lee W.K., Cho S., Jin G., Jheon H.S., Son J.W., Lee M.H., Jung D.K., Cha S.I., Kim C.H., Kang Y.M., Kam S., Jung T.H., Jheon S., Park J.Y. Comprehensive analysis of DNA repair gene polymorphisms and survival in patients with early stage non-small-cell lung cancer. Cancer Sci. 2010 Nov. 101(11):2436-42.
34. Kondo Y., Shen L., Issa J. Critical role of histone methylation in tumor suppressor gene silencing in colorectal cancer. Molecular and cellular biology. 2003. Jan 23(1):206-215.
35. Lee S., Lee H., Kim J. Abberant CpG island hypermethylation along multistep hepatocarcinogenesis. American journal of pathology. 2003. Oct 163(4): 1371-1378.
36. Lin Z., Gao M., Zhang X., Kim Y.S., Lee E.S., Kim H.K., Kim I. The hypermethylation and protein expression of p16 INK4A and DNA repair gene O6- methylguanine-DNA methyltransferase in various uterine cervical lesions. J.Cancer Res Clin Oncol. 2005. Jun; 131(6):364-70.
37. Matallanas D., Romano D., Yee K., Kucerova L., Piazzolla D., Baccarini M., Vass J.K., Kolch W., O’neill E. RassF1A elicits apoptosis through an MST2 pathway directing proapoptotic transcription by the p73 tumor suppressor protein. Mol. Cell. 2007. Sep 21; 27(6):962-75.
38. Maruyama R., Toyooka S., Toyooka K. Abberant promoter methylation profile of prostate cancers and its relationship to clinicopathological features. Clinical cancer research. 2002. Feb 8(2):514-519.
39. Moscicki A. CIN management guidelines in adolescents and young women. Abstracts the International papillomavirus society symposium. April 13-14. 2007. Warsaw. P.17.
40. Muller H., Fiegl H., Widschwendter A., Widschwendter M. Prognostic DNA methylation marker in serum of cancer patients. Ann. N.Y. Acad. Sci. 2004. Jun;1022:44-49.
41. Narayan G., Arias-Pulido H., Koul S. Frequent promoter methylation of CDH1, DAPK, RARB and HIC1 genes in carcinoma of cervix uteri: its relationship to clinical outcome. Molecular cancer. 2003. May13;2:24.
42. Nicol G., Crichton D.N., McDowell H.E. et al. Expression of the Hypermethylated in cancer gene (HIG-1). Is associated with good outcome in breast cancer. Br. J. Cancer. 2001. 14. P. 1878-1882.
43. Ouade B.J., Yang A., Wang Y. et al. Expression of the p53 homologue p63 in early cervical neoplasia. Gynecol. Oncol. 2001.Vol. 80 P. 24-29.
44. Rathi A., Virmani A., Harada K. Aberrant methylation of the HIC1 promoter is a frequent event in specific pediatric neoplasms. Clinical cancer research 2003. Sep1; 9(10 Pt 1): 3674-3678.
45. Reesink-Peters N., Wisman G., Jeronimo C. , Tokumaru C.Y., Cohen Y., Dong S.M., Klip H.G., Buikema H.J., Suurmeijer A.J., Hollema H., Boezen H.M., Sidransky D., van der Zee A.G. Detecting cervical cancer by quantitative promoter hypermethylation assay on cervical scrapings: a feasibility study. 2004. Mol Cancer Res. May; 2(5): 289-95 .
46. Ressler S, Scheiden R, Dreier K et al. High-risk human papillomavirus E7 oncoprotein detection in cervical squamous cell carcinoma. Clin Cancer Res. 2007. Dec 1; 13(23): 7067-7072.
47. Schwartz S.M., Carter J.J., Madelaine M.M. et al. Human papillomavirus 16 and 18 L1 serology compared across anogenital cancer cites. Cancer Research. 2001. Mar 1; 61 (5): 1934-40.
48. Sedjo R.L., Fowler B.M., Sneider A. et al.Folate, vitamin B12, and homocysteine status. Findings of no relation between human papillomavirus persistence and cervical dysplasia. Nutrition. 2003. Jun; 19(6): 497-502.
49. Shivakumar L., Minna J., Sakamaci T. et al. The RASSF1A Tumor Supression Blocks Cell Cycle Progression and Inhibits Cyclin D1 Accumulation. Molecular and Cellular Biology. June 2002. Vol.22. №12. P.4309-4318.
50. Song M.S., Song S.J., Ayad N.G., Chang J.S., Lee J.H., Hong H.K., Lee H., Choi N., Kim J., Kim H., Kim J.W., Choi E.J., Kirchner M.W., Lim D.S. The tumour suppressor RASSF1A regulates mitosis by inhibiting the APC-Cdc20 complex. Nature Cell Biol. 2004. Feb 6(2): 129-137.
51. Vos M.D., Ellis C.A., Elam C., Ulku A.S., Taylor B.J., Clark G.J. RASSF2 is a novel K-Ras-specific effector and potential tumor suppressor. The Journal of Biological Chemistry. 2003. Jul 25; 278(30): 28045-51.
52. Zochbauer-Muller S., Fong K., Virmani A. Abberant promoter methylation of multiple genes in non-small cell lung cancers. Cancer Res. 2001. Jan 1;61(1): 249-255.
53. Yildiz I.Z., Usubutun A., Firat P., Ayhan A., Kucukali T. Efficiency of immunohistochemical p16 expression and HPV typing in cervical squamous intraepithelial lesions grading and review of the p16 literature. Pathol Res Pract. 2007; 203 (6):445-9.
54. Young-Sik Cho, Jeong-Woo Kang, MinChul Cbo et al. Down modulation of IL18 expression by human papillomavirus type 16 E6 oncogene via binding to IL-18. FEBS Letters 2001; 501: 139-45.
Сейчас в России повсеместно используется скрининг-мазок на онкоцитологию (или Пап-тест), а также обычная или расширенная кольпоскопия. Но данные методы, особенно мазок, очень зависят от субъективных факторов.
Современная диагностика предраковых состояний шейки матки.
Рак шейки матки занимает 2 место в мире среди злокачественных опухолей органов репродуктивной системы у женщин, уступая лишь раку молочной железы. Специалисты отмечают негативную тенденцию в отношении заболеваемости раком шейки матки, так как случаи его возникновения в молодом возрасте участились.
Ежегодно в мире выявляют примерно 500 000 новых случаев заболевания, из них 15000 в России.
Причины появления рака шейки матки и факторы риска
В наше время никто не может назвать точные причины формирования злокачественных новообразований. Многие специалисты предполагают, что процесс формирования рака шейки матки длительный (более 8-10 лет), как правило, ему предшествуют предраковые состояния (цервикальные неоплазии – CIN), которые подразделяются на 3 степени. Вероятность перерождения CIN I в рак составляет менее 1% и всего 10% трансформируется в CIN II, 60% подвергаются обратному развитию, а 30% остаются на неизменном уровне. В свою очередь, только 10% CIN II прогрессирует до CIN III, из которой примерно 12-50% случаев на протяжении 3 лет трансформируются в рак, а 30-40% никак себя не проявляют и остаются на всю жизнь.
Многие авторы выделяют ряд предрасполагающих факторов, которые повышают вероятность формирования рака шейки матки, при этом их влияние значительно возросло за последнее годы:
ВПЧ (вирус папилломы человека): у подавляющего большинства онкологических пациентов (90%) был выявлен ВПЧ. Существует более 200 типов этого вируса, среди них особую значимость представляют примерно 13, в частности 16 и 18 виды, на долю которых приходится более 70% злокачественных новообразований.
Раннее начало сексуальных отношений: начало половой жизни в раннем возрасте часто вызывает развитие рака шейки матки. Ведь в этот период ткани недостаточно развиты и подвержены травмированию, что может привести к злокачественным процессам. Научно доказано, что если приступить к половым отношениям до 16 лет, то риск появления опухоли увеличивается в 16 раз, если в 16-19лет – в 3 раза, если в 13-14 лет – в 26 раз.
Беспорядочная половая жизнь: число половых партнеров значительно увеличивает риск заражения ВПЧ, если их 5, то можно говорить о 100% заражении вирусом;
Стадии рака шейки матки и прогнозы выживаемости
Прогнозы выживаемости при злокачественных новообразованиях зависят от множества различных факторов: возраста больных, их общего состояния, сопутствующей патологии и других. Большую роль играют стадии развития опухоли. В среднем пятилетняя выживаемость в мире равна 60%, в Европе – 56%, в России – 55%, в развивающихся странах – 48%.
Шансы на полное выздоровление и сохранения репродуктивного здоровья целиком и полностью зависят от того, на какой стадии цервикальной неоплазии (CIN) или рака начато лечение.
Поэтому особая роль в профилактике рака шейки матки отводится регулярным осмотрам у гинеколога. Женщинам до 35 лет , даже если ничего не беспокоит, 1 раз в год надо обязательно проходить обследование у гинеколога, после 35 лет –дважды в год. Важно осознавать , что упущенное время для обследования и лечения, приводит к серьёзным последствиям. Развитие опухоли в доклиническом периоде, то есть до появления первых признаков, длится годами, поэтому существуют возможности раннего выявления и подтверждения диагноза. А это дает возможность использовать наиболее современные и эффективные методы лечения на самых ранних стадиях заболевания.
В настоящее время появилось уникальное оборудование, позволяющее идентифицировать наличие предраковых и раковых состояний тканей шейки матки на самой ранней стадии заболевания в режиме реального времени при гинекологическом обследовании.

Оптико-электронный сканер TruScreen обеспечивает высокую точность и быстрый результат исследования. Оборудование состоит из ручного зонда и консоли сканера. Консоль сканера TruScreen снабжена микрокомпьютером с установленной программной экспертной системой оценки для анализа и обработки полученных от диагностического зонда данных об исследуемой ткани шейки матки. Процедура занимает 1-2 минуты и абсолютно безболезненна для пациентки.
Сейчас в России повсеместно используется скрининг-мазок на онкоцитологию (или Пап-тест), а также обычная или расширенная кольпоскопия. Но данные методы, особенно мазок, очень зависят от субъективных факторов.
Так, неверными их данные могут оказаться из-за ошибочной тактики взятия мазка. Например, если с этой целью медсестра или врач используют не специальную щеточку или взяли мазок не из зоны трансформации, откуда обычно берет свое начало рак. Или если данные неправильно интерпретированы врачом, выполнявшим исследование полученного материала.
В случае с трускрин-тестом, , ошибки по причине человеческого фактора отсутствуют. Если врач неправильно приложит аппарат к шейке матки, или проработает недостаточно на ней точек, то сканер не выдаст заключение.
Безопасные для человеческого организма электрические и световые лучи, посылающие аппаратом, по-разному отражаются от нормального и атипичного эпителия. И непосредственно устройство интерпретирует полученные данные и дает ответ.
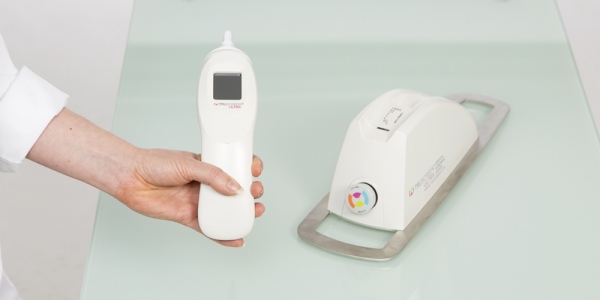
В сканере TruScreen используются одноразовые датчики для более точной диагностики и защиты от инфекций. Тестирование проводится путем легких касаний зондом поверхности шейки. После этого сканер Truscreen автоматически анализирует полученные данные и немедленно распечатывает отчёт на бумажном носителе в одном из вариантов: «Normal» или «Abnormal» (CIN, дисплазия 1—3 степени, инвазивный рак).
Применение систематического комбинированного скрининга TruScreen тест, ПАП-мазок, кольпоскопия позволяет выявить заболевание на стадии предрака, значительно снизив заболеваемость и смертность от рака шейки матки так как вовремя начатое лечение- это шанс на сохранение репродуктивного здоровья и жизни.
В мире около 630 млн человек инфицировано ВПЧ [4]. Большинство женщин инфицируются ВПЧ вскоре после начала половой жизни. Уже через два года после сексуального дебюта до 82% женщин считаются инфицированными ВПЧ [5], при этом даже при одном партнере 20% женщин инфицированы ВПЧ [6]. По данным Всемирной организации здравоохранения, три четверти сексуально активных женщин поражается этим вирусом хотя бы один раз в своей жизни.
Значение скрининга в диагностике предрака и рака шейки матки
Одной из актуальных задач современного здравоохранения является своевременная диагностика предраковых заболеваний и рака шейки матки. Рак шейки матки занимает третье место в мире среди самых распространенных злокачественных новообразований у женщин и является причиной преждевременной смерти сотен тысяч женщин. Ежегодно в мире диагностируют 530 тыс. новых случаев рака шейки матки и более 270 тыс. женщин умирают от данного заболевания. Более 85% смертей приходится на страны с низким и средним уровнем дохода. В развивающихся странах смертность от рака шейки матки выше из-за отсутствия эффективных программ скрининга и ограниченного доступа к медицинской помощи [1].
В России в структуре онкологической заболеваемости женщин преобладают злокачественные новообразования репродуктивной системы (38,8%), при этом 18,1% приходится на опухоли половых органов. В 2012 г. показатель заболеваемости раком шейки матки в нашей стране составил 13,9 на 100 тыс. женского населения. С 2002 по 2012 г. заболеваемость раком шейки матки увеличилась на 26,62%. Рак шейки матки в структуре смертности от злокачественных новообразований в нашей стране является причиной смерти 24% женщин в возрасте от 30 до 39 лет и 13,7% женщин в возрасте от 40 до 49 лет [2].
Рост заболеваемости раком шейки матки обусловлен отсутствием эффективных скрининговых программ, программ профилактики и стандартизованных методов диагностики, недостаточным использованием современных методов диагностики (жидкостная цитология, онкомаркеры) и поздней обращаемостью пациенток к врачам.
Доказано, что заболевания шейки матки, в том числе рак шейки матки, ассоциированы с вирусом папилломы человека (ВПЧ). Именно длительная персистенция ВПЧ в тканях органов нижнего отдела генитального тракта провоцирует развитие предраковых и раковых процессов шейки матки [3]. ВПЧ-ассоциированные заболевания шейки матки встречаются у 50–80% населения и в 99,7% случаев подтвержденного рака шейки матки. Более 15% случаев рака шейки матки диагностируют в возрасте от 20 до 34 лет, что требует поиска новых скрининговых методов исследования для раннего выявления цервикальной интраэпителиальной неоплазии (cervical intraepithelial neoplasia – CIN) и рака шейки матки в этой возрастной группе [1].
В мире около 630 млн человек инфицировано ВПЧ [4]. Большинство женщин инфицируются ВПЧ вскоре после начала половой жизни. Уже через два года после сексуального дебюта до 82% женщин считаются инфицированными ВПЧ [5], при этом даже при одном партнере 20% женщин инфицированы ВПЧ [6]. По данным Всемирной организации здравоохранения, три четверти сексуально активных женщин поражается этим вирусом хотя бы один раз в своей жизни.
- раннее начало половой жизни;
- три и более половых партнеров в течение года и более шести половых партнеров в течение жизни;
- курение;
- употребление алкоголя;
- воспалительные заболевания шейки матки;
- частые роды и аборты;
- авитаминозы;
- низкий социально-экономический уровень жизни;
- иммунодефицитные состояния (ВИЧ);
- трансплантация органов и др.
Скрининг – метод, который используется с целью выявления определенного заболевания или факторов, способствующих развитию данного заболевания, и носит одномоментный или поэтапный характер. Необходимо отличать скрининг от ранней диагностики – выявления заболевания у лиц, которые сами обратились за медицинской помощью после появления у них жалоб и симптомов заболевания.
Цель скрининга рака шейки матки – активное выявление признаков рака шейки матки в преклинической фазе и его лечение органо- и тканесберегающими методами, что позволяет сократить сроки лечения, уменьшить риск инвалидизации и смертности.
Скрининг предрака и рака шейки матки может быть организованным и оппортунистическим. Организованный скрининг более эффективен и экономичен, поскольку разрабатывается на государственном уровне, осуществляется по утвержденной программе и позволяет широко охватить население. Оппортунистический скрининг – обследование женщин, пришедших на прием к гинекологу, – имеет низкую эффективность.
Цитологический скрининг признан классическим методом и рекомендован Всемирной организацией здравоохранения для проведения в масштабах национальных программ.
Впервые цитологический скрининг рака шейки матки был проведен в канадской провинции Британская Колумбия (1949). Затем программы скрининга стали внедрять в других странах мира: в 1950-х гг. – в США и Китае, с начала 1960-х гг. – в Японии, Финляндии, Швеции, Исландии, СССР, с начала 1970-х гг. – в Германии, Бразилии и других странах. В Канаде в результате проведения цитологического скрининга заболеваемость раком шейки матки снизилась с 28,4 случая на 100 тыс. женщин старше 20 лет в 1955 г. до 6,3 случая на 100 тыс. женщин в 1980 г.; смертность уменьшилась на 72%. В Китае с 1958 по 1977 г. частота рака шейки матки снизилась в 10 раз (с 195,3 до 14,8 случая на 100 тыс. женщин). В нашей стране хорошие результаты получены в организованном скрининге, проводимом в медицинских учреждениях Октябрьской железной дороги. За 20 лет (с 1965 по 1984 г.) количество заболеваний инвазивным раком шейки матки снизилось с 31,61 до 8,13 на 100 тыс. женщин (на 74,3%); почти такое же снижение отмечено и в показателях смертности [7].
Во многих развитых странах широкое внедрение скрининговых программ позволило своевременно выявить и назначить адекватное лечение предопухолевых состояний шейки матки, а в результате снизить заболеваемость и смертность от рака шейки матки. При правильно организованном цитологическом скрининге эффективность его достаточно высока. Так, например, в Исландии, где скрининговые программы охватывали почти все возрастные группы (29–59 лет, 90% женского населения), смертность от рака шейки матки за 20 лет уменьшилась на 80%, в Финляндии и Швеции – на 50 и 34% соответственно. В Дании скрининг охватил приблизительно 40% населения, что позволило снизить смертность на 25%. В Норвегии, где только 5% населения принимали участие в скрининге, смертность от рака шейки матки снизилась на 10% [4, 7].
В России в настоящее время организованный скрининг не проводится. Цитологический скрининг предрака и рака шейки матки осуществляется только при диспансеризации, которая вновь стала обязательной с 2013 г. (приказ Минздравсоцразвития России от 04.02.2010 № 55н «О порядке проведения дополнительной диспансеризации работающих граждан» и Федеральный закон от 21.11.2011 № 323-ФЗ «Об основах охраны здоровья граждан в РФ»). Для детей, студентов и ветеранов ВОВ предусмотрена ежегодная диспансеризация, с 21 года рекомендуется обследоваться один раз в три года.
Согласно российским рекомендациям скрининг на рак шейки матки рекомендуется проводить с 25 до 65 лет с интервалами каждые три года у женщин моложе 50 лет и каждые пять лет у женщин 50–65 лет. Вакцинация не является причиной отказа от регулярного скрининга. В обязательном порядке его должны проходить женщины с тотальной гистерэктомией по поводу доброкачественных заболеваний матки, с субтотальной гистерэктомией, с гистерэктомией по поводу инвазивного цервикального рака, с указанием на цервикальные интраэпителиальные неоплазии второй и третьей степени в анамнезе.
- размещение материала не на стекле, а в транспортной жидкости;
- сохранение морфологических, иммуноцитохимических и генетических свойств клеток;
- тонкослойный мазок (он не загрязнен воспалительными и кровяными элементами);
- более высокая чувствительность по сравнению с мазком Папаниколау;
- возможность компьютерной интерпретации большого числа мазков;
- возможность одновременного исследования клеточного материала из одного флакона на ВПЧ (ВПЧ-тест) и цитологию (мазок Папаниколау);
- возможность проведения дополнительных, уточняющих исследований, например выявления иммуноцитохимических биомаркеров p16 и Ki-67.
Для интерпретации результатов цитологического исследования мазков с шейки матки используют классификацию по Папаниколау и терминологическую систему Бетесда (2001).
- первая – нормальная цитологическая картина;
- вторая – изменение морфологии клеток (небольшое увеличение ядра и появление клеток метаплазированного эпителия), обусловленное воспалительным процессом во влагалище и (или) шейке матки;
- третья – единичные клетки с аномалией ядер и цитоплазмы (дискариоз) – подозрение на злокачественное новообразование;
- четвертая – отдельные клетки с явными признаками озлокачествления;
- пятая – большое число типично раковых клеток – диагноз злокачественного новообразования не вызывает сомнений.
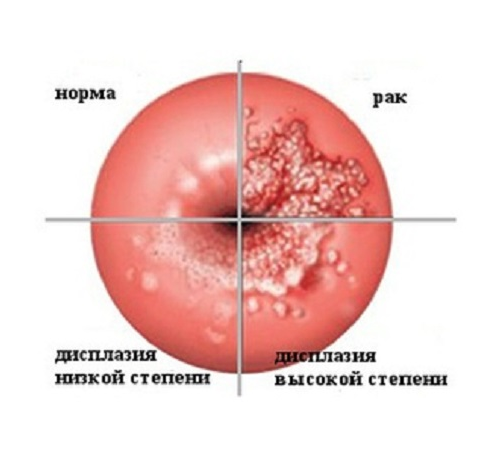
Недостатком данной классификации является то, что в ней не учитываются цитологические изменения, обусловленные ВПЧ. Терминологическая система Бетесда была предложена, когда была изучена роль ВПЧ в генезе рака шейки матки. Согласно системе Бетесда начальным компонентом интерпретации цервикальных мазков является оценка адекватности образца, так как его качество влияет на чувствительность цитологического метода. Система предполагает два вида образцов: удовлетворительный (наличие или отсутствие компонента эндоцервикса/зоны трансформации) и неудовлетворительный.
В системе выделено три категории мазков: норма, мазки неопределенного значения (atypical squamous cells of undetermined significance – ASCUS) и с внутриэпителиальными поражениями (предраковые) низкой (low-grade squamous intraepithelial lesions – LSIL) и высокой (high-grade squamous intraepithelial lesions – HSIL) степени.
В результате подтверждения этиологической роли ВПЧ в развитии рака шейки матки тестирование на ВПЧ стало обязательным элементом скрининга этого заболевания. Во многих клинических исследованиях было показано, что ВПЧ-тест на выявление ДНК-содержащих вирусов дает возможность количественного определения ДНК ВПЧ, вирусной нагрузки, обладает высокой чувствительностью при поражениях высокой степени (80–100%). В США он является обязательным скрининговым методом для женщин после 30 лет.
Другие статьи из блога:
- Женщина без шейки матки
- Где находится шейка матки у женщин
- Выделения при раскрытии шейки матки перед родами
- Праджисан при короткой шейке матки
- Локализация отделяемое влагалища шейки матки уретры
- Полип шейки матки при удаленной матке
- Если удалить шейку матки можно потом родить
- Выпадение шейки матки причины
- Методы диагностики предраковых заболеваний шейки матки
- Оценка зрелости шейки матки алгоритм
Источники и связанные статьи:
